El Lotus japonicus es una planta leguminosa que se utiliza como organismo modelo para estudiar la fisiología y la biología molecular de las plantas leguminosas. No tiene nada que ver con la flor de loto japonesa que es una planta diferente (Nelumbo nucifera). Cabe recordar que las leguminosas son plantas que merced a las bacterias simbióticas que habitan en sus raíces son capaces de fijar el nitrogeno atmosférico, y por tanto, fertilizar el suelo. Esta fijación del nitrógeno atmosférico es uno de los mayores factor limitantes de la agricultura, puesto que forma artificial solo podemos hacerlo por el proceso de Haber-Bosch, en condiciones de alta presión y temperatura y a costa de muchísima energía. Por lo tanto ser capaz de reproducir de forma sintética lo que hacen las bacterias de forma natural supondría aumentar la producción agrícola, lo que justifica los numerosos estudios que hay sobre Lotus. Una de las proteínas importantes en este proceso son las hemoglobinas vegetales.

Evolutivamente las hemoglobinas tienen una historia fascinante, ya que son de las pocas proteínas presentes (directamente o alguna proteína emparentada) en todas las ramas de la vida. Las hemoglobinas tiene un origen ancestral común muy antiguo, en las bacterias, y pasaron a las células más complejas (con núcleo) por transferencia horizontal a partir de las bacterias que vivían dentro de ellas de forma simbiótica. Es decir, que si hoy respiramos es porque en nuestra historia evolutiva un gen de bacterias paso a otro organismo. Somos transgénicos y gracias a ello respiramos. Pero el viaje fue de ida y vuelta. En los nodulos de las leguminosas se encuentran bacterias que tienen hemoglobina, que proviene por trasnferencia horizontal de las hemoglobinas no simbióticas de las plantas. Vamos que lo del cambalache de genes no es algo que hayamos inventado en el laboratorio. También existen proteínas evolutivamente emparentadas con las hemoglobinas como las neuroglobinas, la mioglobina, la flavohemoglobina, la citoglobina etc…
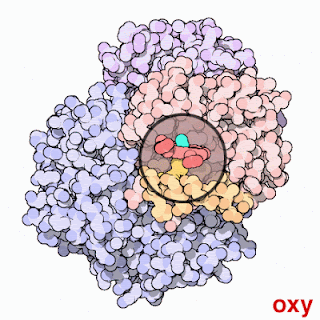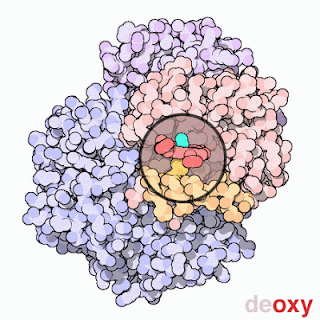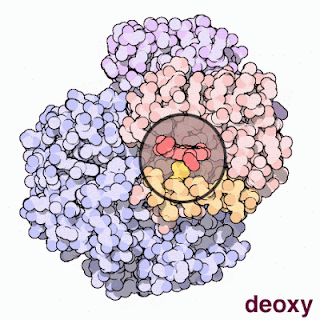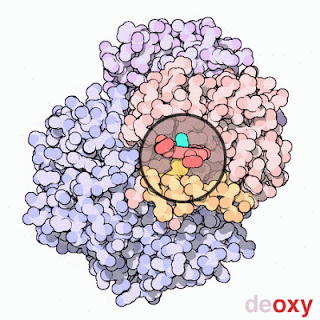
Tenemos la imagen que las hemoglobinas son las proteínas contenidas en los glÓbulos rojos y que su función es llevar el oxigeno y recoger el CO2 de las células, lo cual es cierto, pero es solo una parte muy reducida de la función de las hemoglobinas. Al margen del transporte de gases las hemoglobinas pueden catalizar reacciones químicas, principalmente utilizando especies reactivas de nitrógeno como sustrato, o servir para eliminar determinadas moléculas como oxígeno, CO2 o NO del medio. El principal factor determinante de la función de una hemoglobina será su constante de afinidad por determinados gases. Una hemoglobina con una constante de afinidad muy alta por oxigeno no servirá para transportarlo, ya que atrapará el oxígeno del medio, pero no lo soltará hasta que no haya desaparecido casi por completo. De la misma manera, el monóxido de carbono es tan tóxico porque tiene muchísima afinidad por al hemoglobina, lo que provoca su inactivación. Los cetáceos, para aguantar tanto tiempo debajo del agua tienen además de hemoglobina mioglobina, que tiene muchísima afinidad, lo que provoca que vaya soltando el oxígeno en la sangre a medida que se va agotando el de la hemoglobina. La forma clásica de regular la actividad de la hemoglobina en animales es el alosterismo, es decir, la proteína tiene 4 subunidades (con diferentes variantes según el tipo de la hemoglobina) y la unión de una gas provoca que cambie la afinidad en las otras subunidades.

Para complicar más la cosa en plantas encontramos diversos grupos de hemoglobinas. Por una lado las simbioticas, que las produce la planta en respuesta a la formación de rizobios (interacciones simbióticas con bacterias) y se localizan en estas regiones y las no simbióticas. Seguimos liándolo, dentro de las no simbióticas tenemos 3 tipos, las tipo 1, las tipo 2 y las tipo 3 o truncadas. Las tipo 1 tienen una afinidad por O2 muy alta, por lo que no sirven para el transporte. Se inducen en condiciones de falta de oxigeno, algo que les pasa a las plantas por ejemplo, cuando el campo se inunda. Su función más probable es almacenar oxigeno para darlo en condiciones extremas. También se ha propuesto que pueden participar en la oxidación del NO a nitrito.
Las del tipo 2 tienen afinidades por oxígeno similares a las simbióticas y su función no está demasiado bien caracterizada. Se sabe que se inducen por algunos tipos de estrés ambiental como frío o por hormonas como la citoquinina. También se ha relacionado con la formación de órganos y acumulación de aceite en semillas. Por ultimo tendríamos las tipo 3 o truncadas. La mayoría de las hemoglobinas tienen una estructura de bocadillo 3 sobre 3, en la que 3 hélices aparecen confrontadas a las otras 3 hélices. En estas, como su nombre indica, la secuencia es más corta y la estructura es de dos hélices sobre otras dos.
Por último para estudiar las hemoglobinas conviene saber si el grupo hemo se coordina con cinco aminoácidos o con seis. Que se coordine con seis limita su función porque impide la unión con otros ligandos. Trandicionalmente se ha pensado que las hemoglobinas vegetales no simbióticas están unidas por seis sitios. No obstante no hemos carcaterizado tantas hemoglobinas vegetales para saber si esto es una carcterística común.
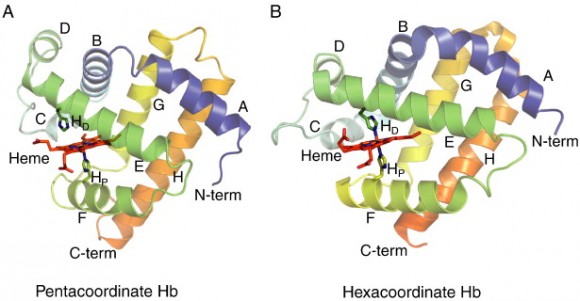
¿Qué pasa en Lotus? Pues tenemos dos hemoglobinas tipo 1, una tipo 2 y dos tipo 3. A diferencia de otras plantas como A. thaliana (la que se suele utilizar en biología molecular de plantas) que solo tiene una de cada grupo. Para caracterizarlas lo primero es meter el gen en una bacteria, aislar la proteína pura y estudiar el espectro de Soret. Esta es una técnica de espectrometría que nos dice si el grupo hemo esta ligado con 5 o con 6 moléculas. Primera sorpresa. Como era de esperar las dos tipo 1 están hexacoordinadas y las tipo 3 pentacoordinada, pero la tipo 2 puede estar de una forma o de otra en función de que el hierro del grupo hemo esté reducido (Fe2+) u oxidado (Fe3+).
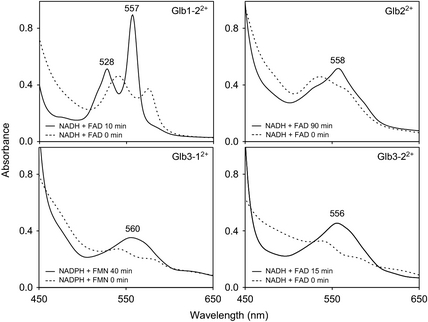
Siguiente paso, medir la afinidad por oxigeno, y aquí es donde viene el récord. GLB1-1 tiene una afinidad por O2 de 50 picomolar, lo que hace la más alta medida hasta la fecha para cualquier tipo de hemoglobina. Es decir que coge el oxígeno y no lo suelta. La otra de la misma familia GLB1-2 tiene una afinidad de 0.9 nm, unas 18 veces menos. Hay algunos compartimentos de la célula donde el oxigeno gaseoso puede ser problemático, por lo que su función sería la de hacerle el abrazo del oso a cualquier molécula de oxigeno que aparezca y no soltarla.

Sigamos con la caracterización ¿dónde se encuentran? Para esto se generaron anticuerpos contra las cinco hemoglobinas de forma que fueran capaces de unirse a la proteína. una vez unidos a la proteína, se incubaron con un segundo anticuerpo que unía al primero, pero este anticuerpo iba trucado con un poco de oro, oro que en el microscopio se ve muy bien, por lo tanto si ves el oro, sabes que es tu proteina. Y parece ser que están predominantemente en el núcleo de las raíces y los nódulos, es decir, en la zona de fijación del nitrógeno. esto supone un problema. Para la mayoría de las funciones la hemoglobina necesita que el hierro esté en forma de hierro 2. Este hierro puede oxidarse espontáneamente por diferentes efectos oxidantes que suceden en las células. Hay diferentes enzimas capaces de reducir el hierro del grupo hemo, pero sabemos que no se encuentran en el núcleo de las células. Bueno, en una célula, para casi todo hace falta una enzima, ¿pero y si no hiciera falta? Resulta que las 5 hemoglobinas no simbióticas de Lotus son capaces de reducirse con moléculas como el NADH o el FAD que pueden de donadoras o aceptoras de protones, conjugadas a una enzima o no. En este caso al reducción se pudo hacer en un tubo de ensayo sin la presencia de enzimas.

Hasta aquí ya sabemos, donde están y que pueden ser funcionales, pero ¿que hacen? La mayoría de los datos son in vitro, es decir, en tubo de ensayo. Nos hace falta alguna evidencia de la funcionalidad in vivo. Una forma es hacer plantas mutantes para estas hemoglobina y ver que pasa o plantas transgénicas que las sobreexpresen. El problema es que hacer plantas transgénicas que sobreexpresen las 5 hemoglobinas hubiera alargado el proyecto demasía. Se puede probar a intentar trabajar en un sistema heterólogo como levadura que nos permite en poco tiempo probar toda una serie de condiciones y comparar en paralelo los 5 genes. Los reultados fueron que GLB2 y GLB3 dan tolerancia a un oxidantes fuerte como Paraquat o cobre, además de a frío. Por su parte GLB2 y GLB1 también dan tolerancia a especies reactivas de nitrógeno. por lo tanto estas 5 hemoglobinas podrían funcionar defendiendo a las raices de la planta de oxidación, ya sea frente a oxígeno o a nitrógeno, y las funciones erían difernetes para cada una, como se demuestra por los datos in vitro (diferentes afinidades por oxigeno) e in vivo (diferente tolerancia).
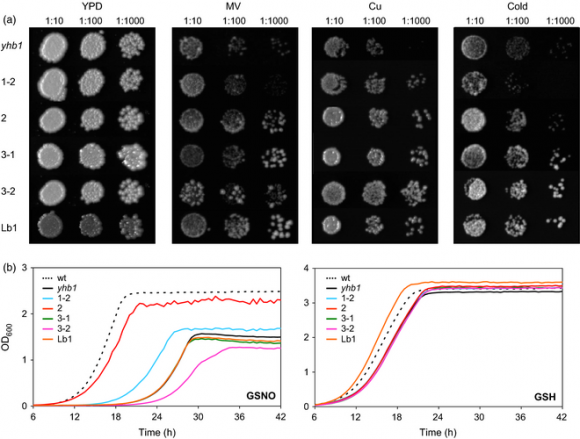
PD: Este estudio ha sido dirigido por el grupo de Manuel Becana, en la estación experimental de Aula Dei en Zaragoza, con al colaboración del grupo de Euan James en en Dundee (Escocia), de Jacob Petrich en Iowa (Estados Unidos) y de un servidor en el IBMCP de Valencia y publicado en la revista Plant Journal.

¿Hablas de plantas mutantes o transgénicas y todavía no hay ningún troll haciendo comentarios estúpidos por aquí sobre los riesgos, la alarma social y todos esos rollos? Casi que no me lo creo…
Buen artículo. Merece una buena lectura en profundidad.
Saludos,
A esa planta la paga MONSANTO!
Algunos errores ,supongo que debidos a no hacer revisión de errores en el texto…
Born-Haber o Haber-Born , no Bosch …
nanomolar es nM, nm es nanómetro…
unos reultados sin s…
raíces sin tilde…
erían sin s…
enhorabuena por tus maravillosos artículos en naukas, sigue así.
Es que el ciclo de Born-Haber es otro. Yo me refiero al proceso de Haber-Bosch para la síntesis de amoníaco:
http://es.wikipedia.org/wiki/Proceso_de_Haber
Gracias por los ánimos, nunca vienen mal.