Muy buenas, soy un pringado estudiante del master del IBMCP. He de hablaros del trabajo que realizo a diario porque no tengo más remedio gustosamente. No voy a contaros mis resultados ya que no tengo casi nada, además son cosas súper importantes, con contratos multimillonarios detrás y que cambiarán la vida a millones de personas, y cobro millones por mantener mi boca cerrada. No debí decir eso… aquí va un tostón para disimular y dar el esquinazo a mis superiores:
<coñazo>
Las giberelinas son una clase de fitohormonas que participan en la regulación de numerosos procesos importantes del crecimiento y desarrollo de las plantas como el mantenimiento del letargo de las semillas o la reducción de la proliferación y expansión celular. Una pieza clave de la ruta de señalización de la hormona son las proteínas DELLA, que son reguladores transcripcionales de localización nuclear que reprimen las respuestas a giberelinas. Aunque las DELLA no se unen directamente al DNA, son capaces de interaccionar con un alto número de proteínas reguladores de diversas familias, típicamente factores de transcripción, lo que explica que sean capaces de controlar tan amplia variedad de procesos. Mi investigación consiste en encontrar proteínas que interactúen con las DELLA y caracterizar dichas interacciones para entender mejor cómo las DELLA contribuyen a regular el crecimiento y el desarrollo de las plantas
</coñazo>
Ahora sí. Mi trabajo consiste en saber si dos proteínas (las DELLA y una serie de proteínas) interaccionan físicamente o no, es decir, si se pegan. Para ello hay dos técnicas ampliamente utilizadas en la biotecnología de plantas, que son las que estoy empleando en mi proyecto:
Doble híbrido en levadura
Empezaremos por decir que un vector es una secuencia de DNA circular que contiene diferentes genes, es decir, diferentes fragmentos de secuencia que darán lugar a diferentes proteínas. Podemos modificar el contenido de estos vectores, así como introducirlos en un organismo u otro (bacterias, levaduras, plantas…)
En esta técnica se trabaja con 2 vectores. Uno de ellos contiene la información que dará lugar a una proteína DELLA. El otro vector contiene la información que dará lugar a la proteína que queremos saber si se une a DELLA o no.
Además, estos vectores contienen más información. El que contiene la DELLA lo llamaremos BD, porque contiene un elemento llamado Binding Domain (en español, dominio de unión), el cual se unirá a una secuencia de DNA determinada de la levadura. El vector que contiene la otra proteína lo llamaremos AD, porque contiene un elemento llamado Activation Domain.
La idea de esta técnica es que BD no puede hacer nada por sí mismo, pero cuando se le une AD, provoca que se sintetice un gen que permite a la levadura sobrevivir en determinadas condiciones
Ahora bien, ¿qué tiene que ver esto de BD y AD con la interacción entre la DELLA y la otra proteína? Muy sencillo, BD está fusionado a la DELLA, es decir, forman una proteína “doble”, son siamesas. De la misma manera, AD está fusionado a la otra proteína. La levadura será “doble híbrido” cuando contenga ambos vectores. Por tanto, el sistema final completo en caso de interacción lo podemos visualizar en la siguiente figura:
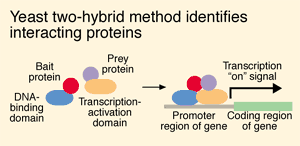
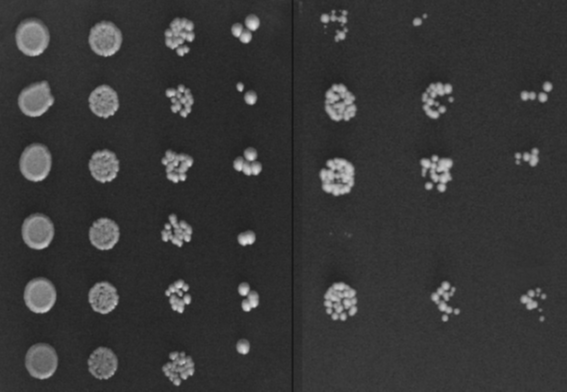
Si DELLA y la otra proteína NO interaccionan (no se unen), no se expresará el gen. Si DELLA y la otra proteína SÍ se unen, BD y AD también estarán próximos físicamente, lo cual permitirá la expresión del otro gen y por tanto la supervivencia de la levadura. En este caso, le permite a la levadura sintetizar un aminoácido que no le suministramos en su medio de crecimiento; con lo cual, si no hay interacción la levadura no crecerá y no podremos observarla.
BiFC
Bimolecular fluorescence complementation, en español, complementación bimolecular fluorescente. Al igual que en el caso anterior, esta técnica nos permite saber si dos proteínas (DELLA y la que queremos saber si se le une) están interaccionando o uniéndose entre sí.
De igual manera en esta técnica hay 2 vectores, uno conteniendo la DELLA y el otro la otra proteína, y de nuevo tanto la DELLA como la otra proteína están fusionadas a otro elemento. Si comparamos con el caso anterior, los elementos al que estaban fusionadas las proteínas permitían en última instancia que se expresase un gen que permitiese sobrevivir a la levadura. En este caso, están fusionadas cada uno a una mitad de una proteína fluorescente (aquella que, si se le aplica una luz determinada, emite otra luz determinada detectable).
Vamos por partes. Las proteínas tienen un extremo llamado C y otro N, no entraremos en más detalles a ese respecto. Nuestra proteína fluorescente se llama YFP (Yellow Fluorescent Protein, en español, proteína amarilla fluorescente, puesto que emite luz amarilla tras aplicarle una determinada luz). Como hemos mencionado, la proteína está dividida en 2 mitades, una parte C y otra N. El vector que contiene la DELLA es el YFC, puesto que contiene la fusión de la DELLA a la parte C de la YFP. El vector que contiene la otra proteína es el YFN, porque contiene la otra proteína fusionada a la parte N de la YFP.

En el caso anterior, los vectores eran introducidos en levaduras. Aquí, se introducen en una bacteria muy especial, Agrobacterium tumefaciens. Esta bacteria tiene gran facilidad para infectar a las plantas en la naturaleza, y se llama así puesto que les causa tumores. No obstante, la bacteria que utilizamos aquí está modificada y es incapaz de causar tumores a la planta, por eso se utiliza mucho para expresar la proteína dentro de las células vegetales de la planta a la que infectamos y ver si se produce la interacción.
En resumen, consiste en conseguir los vectores adecuados, meterlos en Agrobacterium (esto se hace electroporando la bacteria) e infectar la planta con dicha bacteria (se hace por agroinfiltración, esto es, hacer una pequeña herida en la hoja de la planta (normalmente tabaco) e inocular el cultivo bacteriano con una jeringuilla).
Pasados unos días, se aplica luz de una determinada longitud de onda, y al microscopio confocal (utiliza un láser como fuente de luz), podemos ver si se produce la interacción y dónde, dentro de las células vegetales

Y para quien haya llegado hasta aquí, que sepa que este trabajo está mejor pagado que el de Messi (y sólo soy un estudiante!) y que JM no está pagado por Monsanto.
Post realizado por Dani Veintimilla.

Buen post!, lo único que no entiendo es lo de Messi, ¿sarcasmo?
Así es. Lo dije por el tema de que para empezar a ver un duro en este negocio primero hay que pringar a base de bien en la fase de estudiante-semitrabajador, para luego estimar que en unos pocos años hacia el futuro el sueldo difícilmente va a permitir vivir de la ciencia. Se hará lo que se pueda, un saludo Pol
Fantástica explicación. La ciencia no es aburrida y menos cuando está bien explicada, así que no entiendo que califiques el post de tostón o coñazo. Pero tú mismo. Completamente de acuerdo con Pol, los dos últimos renglones sobran en un post tan dinámico y bien explicado.
salud y ánimo con el trabajo.
Me alegro de que te haya parecido más dinámico y entendible que cutre o aburrido 😉 Cuídate Juan
Buen post!!!
El mundo de determinar interacciones entre proteínas es fascinante y hay muchas técnicas disponibles para ello. Yo me he dedicado básicamente a hacer co-inmunoprecipitaciones y aunque puede ser una técnica muy coñazo (hay muchos factores a tener en cuenta que pueden hacer que no veas interacción aunque la haya realmente!!), cuando sale bien es tremendamente satisfactoria.
Sigue así!!
¿Estos datos de itneracción están ya publicados? En la base de datos donde trabajo (www.ebi.ac.uk/intact) recogemos este tipo de información y la preservamos para que pueda ser reutilizada por la comunidad científica y perdure más allá de la vida de tu artículo. Todos los datos de IntAct son de libre acceso y absolutamente gratuitos, es un recurso 100% público.
Ademán, tenemos especial interés en datos de plantas, proque están bastante infrarrepresentados en bases de datos en general. Tener tus interacciones en una base de datos pública aumenta su visibilidad y reusabilidad. Si os interesa enviarlos pre-publicación, dadme un toque y os cuento en más detalle.